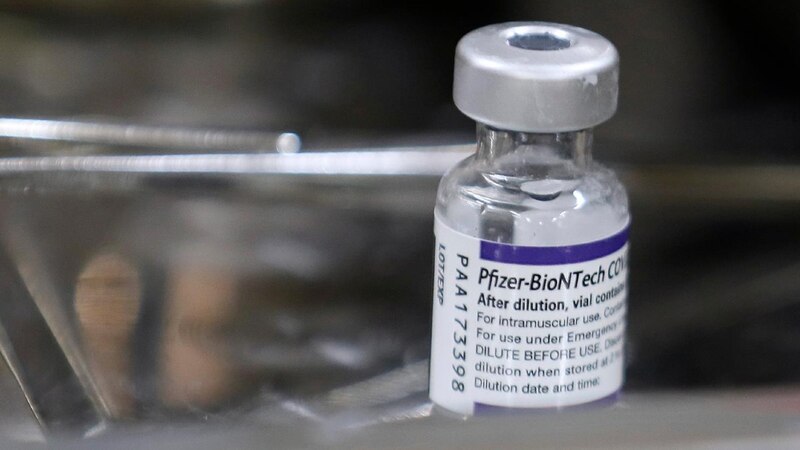
La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) informó que se emitió el aval para la vacuna Comirnaty, de la farmacéutica Pfizer, con lo que se da el primer paso en el proceso de transición del uso de este biológico que fue para su uso de emergencia, durante la pandemia por COVID-19, para contar ahora con su registro sanitario.
El titular de Cofepris, Alejandro Svarch, resaltó que esta transición de autorización de uso de emergencia a registro sanitario “se consolida como un proceso ejemplar para esta autoridad sanitaria. Se realiza en tiempo récord, siendo pioneros en nuestro continente y, sobre todo, aprovechando las herramientas digitales que hemos empleado”.
Lo anterior, luego de que el Comité de Moléculas Nuevas (CMN) evaluó la información técnica y científica proporcionada por Pfizer respecto a la vacuna contra el virus SARS-CoV-2, causante de COVID-19, y como resultado de lo anterior se emitió una opinión favorable, para la vacuna Comirnaty, ARNm monovalente con la actualización de la variante estacional ómicron XBB.1.5 del virus SARS-CoV-2.
Ello, con base en la recomendación de la Organización Mundial de la Salud (OMS), con lo que, el biológico elaborado por Pfizer, da el primer paso en su proceso de transición del “uso de emergencia”, a tener ya su registro sanitario, lo cual permitirá, en caso de completar exitosamente todas las etapas, su comercialización en el mercado nacional.
Lo anterior se dio a conocer, en una sesión pública, en cumplimiento al principio de “caja de cristal”, por lo que se transmitió en vivo la evaluación del referido comité de la Cofepris.
Svarch Pérez, dio inicio de manera formal a estas sesiones públicas; afirmó que se trata de un hecho sin precedentes que tendrá impacto positivo para la salud de la población y resaltó que dicha sesión, fue un evento histórico, porque, es la primera sesión del CMN que se transmite en vivo por redes sociales; esto, en cumplimiento total de nuestro compromiso con la transparencia, siguiendo el principio de caja de cristal utilizado por las principales agencias de referencia del mundo y se trata de un insumo clave para proteger la salud de nuestra población.
Indicó que durante las siguientes sesiones se podrá conocer la información técnica y científica de cuatro vacunas que fueron muy importantes para cubrir las necesidades durante la pandemia de COVID 19, con lo cual se sienta un precedente trascendental para la región.
En esta sesión estuvieron presentes los expertos y expertas del CMN: Alexandra Martín-Onraët Arciniegas, Arturo Galindo Fraga, José Antonio Ortega Martell, José Rogelio Pérez Padilla, Juan Gerardo Sierra Madero y Gustavo Reyes Terán; como observadores de honor, la directora de Prestaciones Médicas del Instituto Mexicano del Seguro Social (IMSS), Célida Duque Molina, y el titular de la Unidad de Educación e Investigación de dicha institución, Víctor Hugo Borja Aburto.
Aunque las sesiones del CMN no son públicas, en cumplimiento al compromiso de total transparencia, por primera vez la población conocerá en vivo las deliberaciones sobre la información técnica y científica de las vacunas contra el SARS-CoV 2.
Cofepris precisó que el CMN es un órgano auxiliar de consulta que forma parte de la agencia reguladora, y su función es emitir opiniones técnicas no vinculantes sobre medicamentos e insumos para la salud, basándose en la evidencia científica y médica presentadas, por lo que, dicho paso no constituye la autorización final para la obtención de registro sanitario.
Copyright © 2023 La Crónica de Hoy .

